- 细胞类
- 生化试剂
- ELISA检测
-
抗体蛋白
二抗生物素标记 过氧化物酶(HRP)标记 胶体金试剂 FITC荧光标记 RBITC荧光标记 二抗免疫血清 其它荧光标记二抗 藻红蛋白(PE)荧光标记 胶体金(Gold)标记 SAlexa Fluor荧光系列 碱性磷酸酶(AP)标记 别藻蓝蛋白(APC)荧光标记 其它标记 PE标记二抗 DyLight标记二抗 AU标记二抗 Biotin标记二抗 AMCA标记二抗 Texas Red标记二抗 TRITC标记二抗 HRP标记二抗 未标记二抗 Cy标记二抗 AbBox Fluor标记二抗内参抗体 小分子抗体抗体标记试剂盒细菌抗体蛋白病毒包装试剂杂交瘤融合筛选WB、IHC、ELISA相关试剂细胞培养试剂病原微生物抗原抗体假病毒抗体校准品其他抗原抗体标记的标签抗体病理级IHC抗体重组蛋白
- 细胞培养
- 实验耗材
- 仪器设备
- 生化试剂盒
- 小分子试剂
- 基质胶
-
斑马鱼产品
订货时间:周一至周五
订货Q Q:79688691
订货邮件:79688691@qq.com
 产品简介
产品简介此试剂盒主要通过纤维素酶和离析酶消化植物细胞壁,再经过滤洗涤去除杂质获得原生质体,通过聚乙二醇(PEG)法进行原生质体融合。适用于从30 d的拟南芥幼苗中分离原生质体。获得的原生质体可用于蛋白的亚细胞定位,验证蛋白间的相互作用,转录因子的转录调控等。本试剂盒包含原生质体制备和转化需要的全部试剂,按照每次10 mL酶解液的使用量,可供10次原生质体制备以及240 个转化反应。
 产品组成成分
产品组成成分| 组分编号 | 组分名称 | 10T | 储存温度 | |
| A盒 | F17385-1 | 酶解缓冲液 EC(Buffer EC) | 80 mL | -20℃ |
| F17385-2 | 酶 E1(Enzyme 1 | 1.5 g | ||
| F17385-3 | 酶 E2(Enzyme 2) | 0.35 g | ||
| F17385-4 | BSA(10%) | 2.5 mL | ||
| F17385-5 | AMP(100 mg/mL) | 1 mL | ||
| B盒 | F17385-6 | 培养液 CM(Buffer CM) | 120 mL×6 | RT |
| F17385-7 | 重悬液 RS(Buffer RS) | 30 mL | ||
| F17385-8 | 转化液 TP(Buffer TP) | 36 mL | ||
| F17385-9 | 还原剂(β-me) | 100 µL | ||
| F17385-10 | 细胞筛 | 10 个 | ||
 使用说明(仅供参考)
使用说明(仅供参考)一、准备工作
1. 需要自行准备的材料:
锋利刀片;血球计数板;50 mL 离心管;2 mL 离心管,切过尖的灭菌蓝枪头和黄枪头、10 μL 白枪头(进口的更佳)。
2.酶解液配制:
| 配制顺序 | 组分 | 10mL体积 |
| 第一步 | 酶解缓冲液 EC | 8mL |
酶 E1(Enzyme 1) | 0.15g | |
酶 E2(Enzyme 2) | 0.03g | |
第二步 | 混匀后 55 ℃水浴 10 min,期间颠倒混匀 2-3 次, 冷却室温后加入以下成分 | |
第三步 | BSA(10%) | 100µL |
还原剂 | 3.57µL | |
Amp(100 mg/mL) | 5µL | |
| 第四步 | 加去离子水定容 | |
第五步 | 过滤除菌(可选步骤) |
注:
1. 酶解液必须现配现用。
2. 根据实验的需要选择酶解液是否需要过滤除菌。
3. 将培养液CM放在冰上预冷,便于后续使用。
二、原生质体的分离制备
1. 准备30d的拟南芥幼苗,优选第 2、3 和 4 对叶片(黄化的原生质体更稳定)。建议使用无菌播种得到的拟南芥幼苗,效果更佳。
注:若使用土培苗,最好用无菌 ddH2O 冲洗擦干后使用,减少细菌的繁殖。
2. 取10-20个拟南芥叶片(样品量约1g,可适当增加),用锋利刀片平行主叶脉,切成 0.5-1.0 mm的细丝。
3. 将切好的细丝放入装有10 mL酶解液的50 mL 容积的小烧杯中,锡箔纸包裹,烧杯口留洞。
注:避光步骤可防止原生质体重新生长出细胞壁,植物细胞壁不利于后续转化。
4. 避光 28 ℃,45 rpm 摇床上孵育3-4 h。收集原生质体前,80 rpm 摇动5 min,让原生质体完全释放出来。
5. 用 1 mL 培养液CM润洗细胞筛后,弃废液。
6. 将酶解后的产物用细胞筛过滤,用镊子或无菌枪头轻轻挤压酶解物帮助充分释放原生质体,此时肉眼可见浓绿色液体滴落(挤压步骤十分重要)。用5 mL 的培养液CM冲洗酶解器皿和未消化的叶片2次(用切过尖的蓝枪头冲洗),将所有的液体收集到一个50mL离心管中。
可选:也可以在第一次过滤后,小心将植物组织转移到锥形瓶中,加入10mL的培养液CM,在28 ℃摇床80 rpm 摇动5min,第二次过滤后,再用5 mL培养液CM冲洗酶解器皿和未消化的叶片2 次。二次重悬过滤可以一定程度提高原生质体的产率,增加转化数。
注:1. 操作过程尽可能轻柔,避免剧烈震荡,过滤时可以将50 mL 离心管倾斜70°,可以缓冲溶液下落时产生的碰撞力,防止原生质体破碎。2. 黄化苗酶解后的原生质体不呈绿色,过滤完成后,可以取一滴酶解液镜检,如果细胞圆而发亮,则健康,可继续进行实验;如果细胞扁且发黑,则弃去。
7. 选用水平转子,室温100 g离心3 min,升速3,降速3,去除上清(管中绿色沉淀即为原生质体)。
注:离心时,可调低离心机的升速和降速。升速过快,原生质体可能离到管壁上导致破碎;降速过快,可能导致管底原生质体悬起。且过快的升降速会使原生质体破碎。建议升速和降速分别都使用 3。
8. 加入10 mL培养液CM温柔重悬位于底部的原生质体(切过尖的蓝枪头),100 g 离心 3 min, 升速 3,降速 3,去上清。
9. 加入1 mL培养液CM,重悬原生质体,冰上避光静置30 min。
10. 在离心前,可以显微镜下观察原生质体的状态和血球计数板计数。
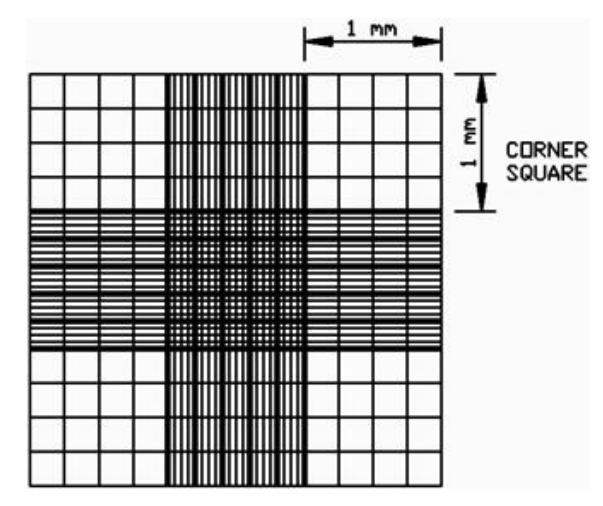
血球计数板的使用:
如下图所示,在血球计数板上加上一个盖玻片,分别从两侧凹槽加入样品。使用中央区域长和宽都是 1 mm的方形区域进行计数(25 个中方格)。分别统计正方形四个顶角和中央 的小正方形的细胞数量,取平均值再乘以 25(正方形被分成了 25 个小正方形),计算该区域的细胞数量,该区域的体积为 0.1 µL(长 1 mm,宽 1 mm,高 0.1 mm)。计算获得的细胞数量。原生质体浓度(个/mL)=25 个中方格原生质体数×104×稀释倍数。
11. 100 g离心3 min,升速3,降速3,去上清,用相应体积的重悬液RS重悬原生质体,调整原生质体密度为2×105 /mL。(根据细胞数量和所需反应数,加入对应的重悬液RS 体积,100 μL/1 个反应)
三、原生质体的转化
1. 在2 mL的灭菌圆底离心管中加入3-20 µg(总体积不超过10 µL,根据实验需要用无菌ddH2O 补齐)纯化后的高质量质粒(建议去内毒素),随后加入100 µL 调整好浓度的原生质体,轻弹充分混匀。
2. 加入110 µL 的转化液TP,轻弹混匀或切过尖的蓝枪头轻轻吸打混匀,过程中应避免产生气泡,室温孵育3-30 min(常规实验不超过15 min)。
注:去内毒素质粒对转化效率有极明显提升(近3 倍),建议购买去内毒素质粒大提试剂盒(吸附柱法)。转化液TP较难溶解,需65 ℃水浴完全溶解后(约 10 min),冷却至室温后使用。原生质体与转化液TP较难混匀,请耐心缓慢的吸打,以至充分混匀,保证转化效率。
3. 加入500 μL 培养液CM,轻柔颠倒混匀,终止转化。室温100 g 离心2 min,升速降速3,在不损失原生质体的情况下,尽可能去上清。
4. 加入500 μL 培养液CM重悬原生质体,室温100 g离心2 min,升速3,降速3,去上清。
四、原生质体的培养和收集
1. 加入500 μL 培养液CM培养悬浮细胞。将离心管水平室温避光放置,孵育 12-16h。
2. 收集细胞时,缓慢拿起离心管,用枪头将附着在管壁上的细胞轻轻悬起,离心管室温垂直静置3 min后再离心,室温100 g离心2 min,升速3,降速 3,去除大部分培养液 CM,收集原生质体,用于后续实验。
 储存与保存
储存与保存1.A盒:-20℃,储存。
2.B盒:常温,储存。
 注意事项
注意事项1. 分离制备的原生质体没有细胞壁的保护,非常脆弱,整个实验操作过程中动作尽可能轻柔。
2. 为了避免原生质体离心时贴在管壁,建议整个实验过程使用水平转子。
3. 实验过程中尽可能使用切过尖的1 mL蓝枪头,保证平滑。因为其尖端的孔径较大,会避免原生质体破裂。
4. 若无水平转子,可适当调整离心力、离心时间、升降速,以保证实验成功。
5. 转化时建议添加空载荧光对照,以验证操作步骤无问题。
6. 土培的成株期植株的组织分离效果会偏差,属于正常现象
7.我司生产的生化试剂如无特殊标注,基本为非无菌包装,若用于细胞实验,请提前做好预处理。需低温保存的产品,一旦配成溶液,请分装保存,避免反复冻融造成的产品失效。
8.本产品仅供科研使用。请勿用于医药、临床诊断或治疗,食品及化妆品等用途。请勿存放于普通住宅区。
9.为了您的安全和健康,请穿好实验服并佩戴一次性手套和口罩操作。
10.实验结果可由多种因素影响,相关处理只限于产品本身,不涉及其他赔偿。
备注:由于产品信息可能会有优化升级,请以实际收货标签信息为准。